Фенилаланин е протеиногенна, незаменима аминокиселина с ароматен шестчленен пръстен, който действа като градивен елемент за много протеини и пептиди.
Фенилаланинът също играе важна роля в азотния метаболизъм и може да се превърне в черния дроб в протеиногенна аминокиселина тирозин. Фенилаланинът и тирозинът играят важна роля в синтеза на инсулин, меланин, тироксин и невротрансмитери допамин, серотонин и тирамин.
Какво е фенилаланин?
Фенилаланинът е основна алфа-аминокиселина, която - за разлика от повечето протеиногенни аминокиселини - е не само биоактивна в L-формата, но в ограничена степен и като енантиомер в R-формата.
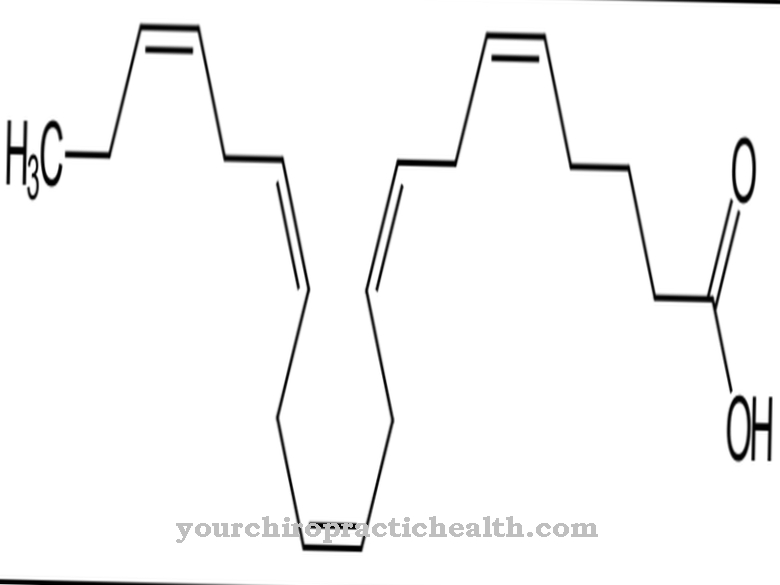
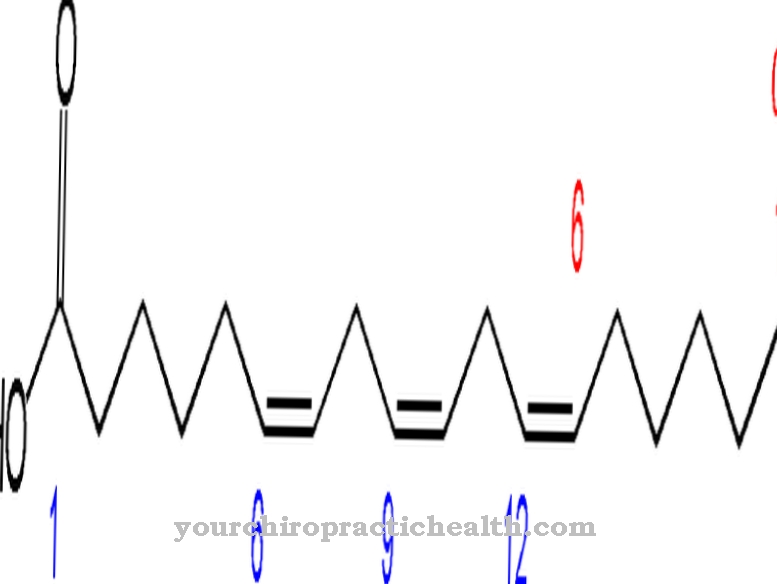
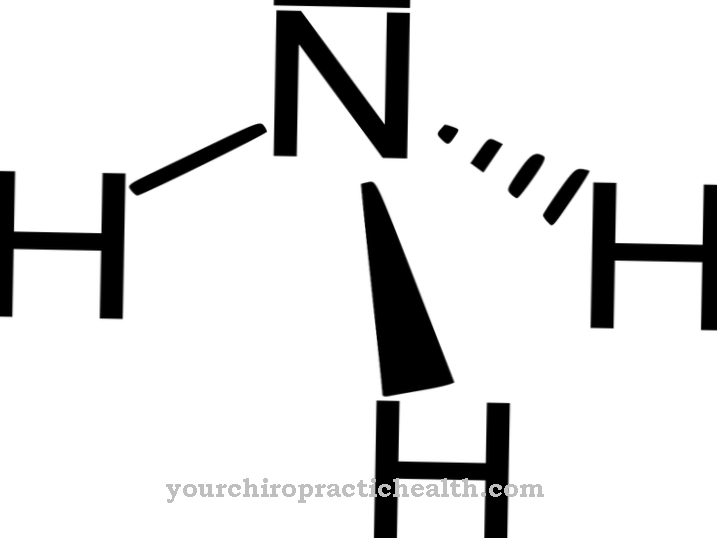
R-фенилаланинът е биохимично до голяма степен неактивен и възниква изключително по време на изкуственото производство на аминокиселината, но ролята на D-фенилаланин в контрола на някои невротрансмитери в болковия комплекс се обсъжда. Като характерна структурна характеристика фенилаланинът има обикновен ароматен шестчленен пръстен (бензолен пръстен) с прикрепена въглеводородна верига. Химическата структурна формула е C6H5-CH2-CH (NH2) -COOH, като C6H5 групата показва бензолния пръстен. Аминокиселината е амфифилна, което означава, че е разтворима както в мазнини, така и във вода.
Химичната формула показва също, че фенилаланинът се състои изключително от въглерод, водород, азот и кислород, вещества, които са повсеместни. Редките метали, минерали или микроелементи не са част от аминокиселината. Въпреки това човешкият метаболизъм не може да синтезира фенилаланин в достатъчна степен от тирозин, а зависи от приема на храна. Фенилаланинът присъства в достатъчни количества в много животински и растителни храни, така че няма нужда да се страхувате от недостиг на аминокиселина при нормална, смесена диета - при условие че храносмилателният тракт се усвоява нормално.
Функция, ефект и задачи
Най-важната функция и задача на фенилаланин е да участва в структурата на много протеини и пептиди. Той участва и в синтеза на някои хормони, които играят централна роля в контрола на метаболитните процеси.
Има хормони като адреналин, норепинефрин, L-допа, PEA и меланин. В допълнение, L-фенилаланинът служи като основно вещество, от което z. Б. може да се синтезира пратеното вещество допамин, серотонин, тирамин и други. L-фенилаланинът също служи като изходен материал за основната аминокиселина тирозин. За тази цел фенилаланинът се превръща в тирозин в черния дроб на два етапа чрез хидроксилиране и чрез разделяне на водна молекула. Фенилаланин хидроксилаза е ензимът, който катализира превръщането в тирозин.
Алтернативно снабдяване с също необходимата аминокиселина тирозин може - както при фенилаланин - да се осъществява чрез прием на храна. За разлика от всички други аминокиселини, които показват само биоактивни ефекти в своята L-форма, D-енантиомерът на фенилаланин изглежда има най-малко влияние върху възприемането на болката. Установено е, че смес от L- и D-фенилаланин (рацемична смес) има аналгетичен ефект. DL сместа вероятно ще блокира разграждането на енкефалините - собствените опиоиди на организма - така че аналгетичният ефект да се удължи и засили.
Образование, поява, свойства и оптимални стойности
Основната аминокиселина фенилаланин се абсорбира чрез храната. Той не е безплатен, но обикновено като част от протеин или полипептид в химически свързана форма. За да се направи аминокиселината достъпна за метаболизма, съответният протеин първо трябва да се разгради в процеса на храносмилането и след това да се екстрахира от "фрагментите", като се използват допълнителни ензими в по-нататъшния метаболизъм.
L-фенилаланинът се синтезира по така наречения път на шикимовата киселина. Това е сложна биокаталитична верижна реакция, която имат автотрофните растения и бактерии. Особеността на автотрофните организми е способността им да образуват органична материя от изключително неорганичен материал. Безплатният L-фенилаланин има горчив вкус, докато D-енантиомерът, който се произвежда изключително в промишленото производство, има сладък вкус. Аминокиселината е z. Б. предлага се като хранителна добавка и също е част от изкуствения подсладител аспартам. Бионаличният L-фенилаланин се намира в обвързана форма в много храни.
Съдържанието им е особено високо в сушен грах и соя, в орехи и тиквени семки, както и в различни видове риба и месо. Изискването за фенилаланин силно зависи от доставката на тирозин. Ако в диетата няма тирозин, тялото се нуждае от 38 до 52 mg на kg телесна маса. С богатото предлагане на тирозин в диетата, дневната потребност спада до едва 9 mg на kg телесна маса. По правило храните, съдържащи фенилаланин, също съдържат съответно количество тирозин.
Препоръката на FAO / WHO от 1985 г. представлява комбинирано изискване за L-фенилаланин и L-тирозин от 14 mg на kg телесна маса на ден. Следователно възрастен с телесна маса 80 кг се нуждае от 1,120 mg от двете вещества дневно.
Болести и разстройства
Симптомите на дефицит, когато трайно е недостатъчно снабдяването с фенилаланин и тирозин в храната, са изключително редки, но могат да имат сериозни последици, особено в областта на невроните.
Освен нарушение на синтеза на много хормони и невротрансмитери, дефицитът може да бъде индикиран и от нарушаване на миелинизацията на нервните влакна. Обратното на дефицит може да възникне свръхконцентрация на фенилаланин (фенилкетонурия) поради генетично метаболитно разстройство. Заболяването се наследява по автозомно рецесивен начин и води до намалено производство на ензима фенилаланин хидроксилаза, който може да превърне фенилаланин в тирозин.
Намалената ензимна активност води до силно повишаване на аминокиселината до това, което е известно като фенилкетонурия, тъй като превръщането в тирозин също е пътят на разпадане на фенилаланин. В същото време липсва тирозин, тъй като пътят на синтеза е блокиран. Друго наследствено заболяване в този контекст е синдромът на Hartnup. Това е метаболитно разстройство, което нарушава транспортирането на фенилаланин през клетъчната мембрана. Това води до сериозни проблеми в ЦНС, по кожата и в храносмилателния тракт.

.jpg)



.jpg)


.jpg)









.jpg)