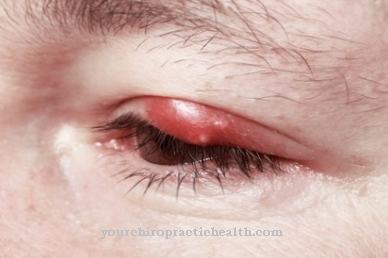
Най- Деоксигениране е дисоциацията на кислородните молекули от молекулите на хемоглобина в човешката кръв. Подаването на кислород в организма се основава на цикъл на оксигенация и дезоксигенация. Този цикъл е нарушен от явления като отравяне с дим.
Какво е дезоксигениране?

При химическа дезоксигенация кислородните атоми се освобождават от атомна връзка. Медицината обозначава термина за разпадането на кислородните връзки върху хемоглобина. Хемоглобинът е червеният кръвен пигмент, който съдържа двувалентни железни атоми. При човешкото дишане хемоглобинът служи като транспортна среда благодарение на тази железна връзка с афинитет към кислорода.
Всички органи и тъкани в тялото се нуждаят от кислород. Кръвта транспортира кислородните атоми до най-тънките клони на кръвообращението и по този начин снабдява всички тъкани.
Кислородът има само ограничена разтворимост. Следователно той не присъства само в кръвната плазма в свободна, но и в хемоглобинова форма. Тази връзка също се нарича оксигенация и е противоположна на дезоксигенацията.
Афинитетът на свързване на хемоглобина към кислорода се променя в различната среда на тялото. Когато афинитетът спадне, се извършва дезоксигениране. Кислородните атоми се отделят в отделните тъкани и органи на тялото. Свързващият хемоглобин се нарича още дезоксихемоглобин. По подобен начин свързаният с кислород хемоглобин се нарича оксихемоглобин.
Функция и задача
Оксигенирането и дезоксигенирането работят заедно в човешкия организъм, за да снабдяват тъканите с жизненоважен кислород. Физически разтвореният кислород играе роля например в обмена между кръвната плазма и алвеолите на белите дробове. Кислородният обмен се осъществява между плазмата и интерстициума чрез дифузия. Физически разтвореният кислород също играе роля в този процес.
За да се поддържа доставката на кислород към всички клетки, обаче, поради ограничената разтворимост, свързването с хемоглобина също е жизненоважен процес. Когато хемоглобинът е кислороден, неговата конформация се променя. С тази промяна в позицията централният железен атом се пространствено пренарежда в червения кръвен пигмент и хемоглобинът придобива динамично функционално състояние.
Без свързване с кислород хемоглобинът всъщност е дезоксихемоглобин и по този начин има напрегната Т-форма. С оксигенацията формата на хемоглобина се променя до спокойна R-форма. Тогава говорим за оксихемоглобин. Афинитетът на хемоглобина към кислорода се променя със съответната форма и пространствено разположение на молекулите. В своята спокойна форма червеният кръвен пигмент има по-голям афинитет към кислорода, отколкото в напрегнатата му форма.
Стойността на pH също оказва влияние върху афинитета. Колкото по-висока е стойността на рН в съответната среда на тялото, толкова по-висок е афинитетът на свързване с кислород на хемоглобина. В допълнение, температурите влияят върху свойствата на свързване. Например, афинитетът на свързване към кислорода се увеличава с намаляването на температурата.
Освен това афинитетът за свързване с кислород зависи от съдържанието на въглероден диоксид. Тази зависимост от концентрацията на въглероден диоксид се нарича заедно с рН зависимостта като ефект на Бор. Афинитетът на свързване на хемоглобина към кислорода спада с увеличаващите се нива на въглероден диоксид и ниска стойност на рН. С ниско ниво на въглероден диоксид и висока стойност на рН афинитетът се увеличава. Поради тази причина хемоглобинът оксигенатира в алвеоларните капиляри на белите дробове по време на дишането, тъй като има спадащо съдържание на въглероден диоксид и pH на кръвта се повишава.
В кръвната система на останалата част от тялото обаче има сравнително високи концентрации на CO2 при ниски стойности на рН. Афинитетът на свързване на червения кръвен пигмент намалява. Кислородът се дисоциира от молекулите на хемоглобина и се извършва дезоксигениране.
Без дезоксигенация, следователно кръвта не би била ефективна транспортна среда за кислород. Ако молекулите на кислорода остават трайно свързани с желязото в хемоглобина, нито телесните тъкани, нито органите биха се възползвали от транспорта.
Болести и неразположения
В случай на отравяне с въглероден оксид, функцията за свързване на кислорода на хемоглобина е нарушена. Ако например пациентът е вдишвал твърде много димен газ при пожарен сценарий, въглеродният окис се отлага върху железните молекули на хемоглобина вместо кислород. В резултат на това в плазмата има по-малко оксихемоглобин. В тялото почти няма оксигенация, защото кислородният афинитет на червения кръвен пигмент пада с концентрацията на СО. Деоксигенирането на хемоглобина се благоприятства с падащия афинитет. Настъпва хипоксия. Тогава тялото вече не е достатъчно снабдено с кислород.
В случай на тежко отравяне се говори за аноксия. Едно такова явление е пълната липса на кислород в тъканите на тялото. Докато аноксията почти винаги е свързана с вдишването на дим, причината за хипоксията също може да бъде анемия или емболия. Например, пациенти със сърповидно-клетъчна анемия страдат от хронична анемия. Вашият анормален хемоглобин има склонност да се слепва, запушва кръвоносните съдове и вече не оксигенира правилно. Следователно сърповидно-клетъчната анемия също може да причини хипоксия. Същото се отнася и за така наречената алфа таласемия, при която синтезът на алфа веригите в протеиновия компонент на хемоглобина е нарушен.
В условията на хипоксия винаги има нарушен клетъчен метаболизъм в организма. Клетките на тялото винаги се увреждат от недостатъчното снабдяване с кислород. Тежестта на последствията от неадекватното снабдяване зависи например от това колко бързо може да бъде отстранено. Приемането на кислород е важна стъпка в лечението на повечето недостатъци. Преливането на кръв обикновено е от съществено значение при заболявания на кръвообращението или разстройства на хемоглобина.










.jpg)

.jpg)